Co to jest masa atomowa?
W chemii masa atomu, która składa się z całkowitej masy protonów i neutronów, nazywana jest masą atomową.
Masa atomowa różni się od masy atomowej, względnej masy atomowej, liczby atomowej i liczby masowej lub liczby masowej.
Masa atomowa jest przedstawiona w układzie okresowym pierwiastków. Przyjrzyjmy się poniżej przykładom .
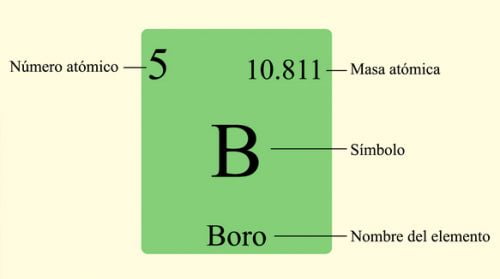 Przedstawienie masy atomowej pierwiastków w układzie okresowym.
Przedstawienie masy atomowej pierwiastków w układzie okresowym.  Masa atomowa tlenu, aluminium i węgla w układzie okresowym.
Masa atomowa tlenu, aluminium i węgla w układzie okresowym.
Jednostki masy atomowej
Jednostką miary masy atomowej jest „amu”, co jest skrótem od „atomic mass units”. Znany jest również jako „u”, co jest skrótem od „zunifikowanych atomowych jednostek masy”, oraz jako „Da”, co oznacza „Dalton”.
Jednostka ta jest zdefiniowana jako 112 część atomu węgla 12 (C-12). Tak więc 1 amu odpowiada 1,66053904 x 1024 gramom.
Na przykład , atom węgla 12 (C-12) w szczególności ma 12 atomowych jednostek masy (u=12).
(tixagag_6) Masa atomowa
Masa atomowa jest zdefiniowana jako średnia masa atomowa wszystkich izotopów danego pierwiastka.
Na przykład , masa atomowa węgla, która jest obliczana na podstawie średniej pomiędzy różnymi izotopami węgla, takimi jak C-12 i C-14, wynosi 12,0107.
(tixagag_6) Liczba atomowa
Liczba atomowa odpowiada liczbie protonów zawartych w każdym atomie pierwiastka. Jest on reprezentowany przez literę Z. Na przykład
, liczba atomowa węgla (C) wynosi 6 (Z=6).(tixagag_6) Numer masy
liczba masowa lub liczba masowa odnosi się do całkowitej liczby protonów i neutronów w jądrze atomu.
Względna masa atomowa
Jeżeli chcemy obliczyć masę atomową pierwiastka, a nie tylko atomu, mówimy o względnej masie atomowej i jest ona reprezentowana przez skrót „Ar”. Zobaczmy.
Pierwiastki mogą występować w przyrodzie w różnych formach, co z chemicznego punktu widzenia oznacza, że mogą składać się z kilku izotopów.
Izotopy oznaczają atomy z różną liczbą neutronów, ale taką samą liczbą protonów. Dlatego masa każdego izotopu jest inna. Tak więc względna masa atomowa odpowiada średniej mas izotopów każdego pierwiastka.