Co to jest jonizacja:
Jonizacja to proces przemiany, zarówno chemicznej jak i fizycznej, w wyniku którego powstają jony .
Jony to atomy lub molekuły, które zawierają ładunek elektryczny z powodu braku lub nadmiaru elektronów w stosunku do neutralnego atomu lub molekuły.
Jonizacja jest również związana z dysocjacją elektrolityczną, zjawiskiem, poprzez które powstają również jony.
Gatunek chemiczny, który posiada więcej elektronów niż neutralny atom lub molekuła nazywa się anionem, a jego ładunek netto jest ujemny. W przeciwnym przypadku, gdy posiada mniej elektronów, nazywany jest kationem, a jego ładunek netto jest dodatni.
Jony, zarówno dodatnie jak i ujemne, występują zarówno w przyrodzie, jak i w materiałach syntetycznych, urządzeniach elektrycznych, odzieży itp.
dodatnio naładowane jony są odpowiedzialne za przenoszenie ładunków statycznych, czyli wyładowań elektrycznych, które odczuwamy, gdy dotykamy metalowego przedmiotu lub nawet innej osoby.
Nadmierna ilość jonów dodatnich ma negatywny wpływ na ludzi, roślinność i zwierzęta.
Z drugiej strony, jony ujemne mają odwrotne działanie: powodują odprężenie i dobre samopoczucie. Na przykład w wodospadach i ich zderzeniu wytwarzane są jony ujemne, które będąc wolne w powietrzu można wdychać i korzystać z ich dobrodziejstw.
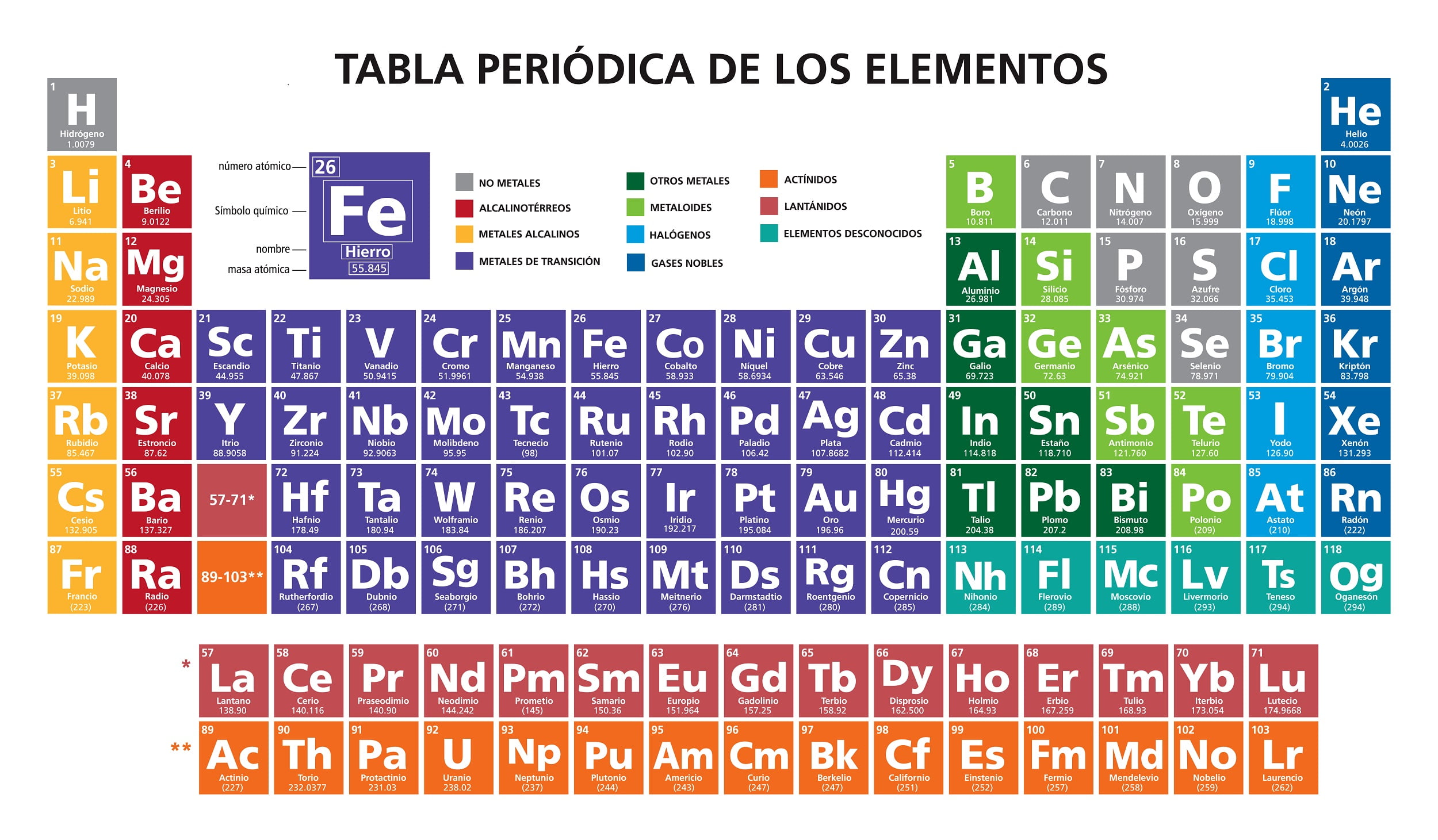
Jonizacja może być zarówno chemiczna jak i fizyczna. Chemiczna jonizacja może przebiegać w różny sposób, m.in. przy silnej różnicy elektroujemności reagujących pierwiastków lub poprzez przeniesienie elektronów, np. gdy chlor reaguje z sodem i powstaje chlorek sodu.
Fizyczna jonizacja polega na wyodrębnieniu elektronów tworzących neutralną cząsteczkę poprzez dostarczenie energii, np. poprzez promieniowanie rentgenowskie, promieniowanie gamma lub światło ultrafioletowe.
Patrz również:
- Co to jest jon?
- Jonosfera.
Energia jonizacji
Energia jonizacji lub potencjał jonizacji odnosi się do ilości energii, która jest dostarczana do neutralnego, gazowego atomu w stanie podstawowym , aby usunąć najsłabszy zachowany elektron i przekształcić go w gazowy kation jednododatni.
Energia jonizacji służy do uzyskania obliczenia, za pomocą którego można zmierzyć przejścia elektroniczne.
Dlatego odnosi się do minimalnej energii potrzebnej do usunięcia elektronu z atomu lub molekuły tak, że nie ma interakcji pomiędzy jonem a elektronem.
Energia zjonizowana rozwija się w sposób stopniowy, ponieważ elektrony opuszczają się w określonej kolejności. Jako pierwsze odchodzą elektrony walencyjne, które są najbardziej oddalone od jądra, a następnie podążają za nimi elektrony wewnętrzne, zmieniając odpowiednio energię do wykorzystania w każdej fazie.
Energia jonizacji może być mierzona w następujący sposób:
- elektronowolty na atom (eV atom)
- Kilokalorie na mol (kcalmol)
- Kilodżul na mol (KJmol)
- Potencjał jonizacji, potencjał w woltach (V) potrzebny do uruchomienia elektronu.
Stała jonizacji
Stała jonizacji jest znana również jako stała dysocjacji kwasu i odnosi się do równowagi odpowiadającej reakcji dysocjacji pomiędzy słabszą zasadą.
Warto wspomnieć, że termin dysocjacja w chemii odnosi się do procesu, w którym mniejsze cząsteczki, jony lub rodniki są oddzielane od cząsteczek lub soli.
Jonizacja wody
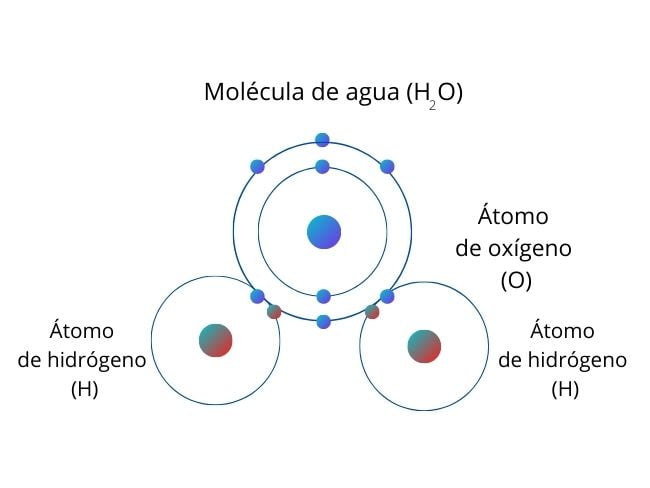
Czysta woda jest słabym przewodnikiem prądu, ponieważ bardzo słabo jonizuje. To znaczy, że woda w stanie czystym jest słabym elektrolitem, który w stanie niskiej równowagi dysocjuje na jony wodorowe H3O+ i wodorotlenkowe OH-.
Wynik ten nazywany jest iloczynem jonowym wody, a jego znaczenie polega na tym, że stanowi on podstawę do stworzenia skali pH, za pomocą której mierzy się kwasowość lub zasadowość roztworu cieczy, czyli stężenie jonów.
Patrz również pH.