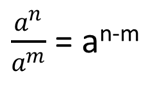Co to jest masa molowa:
Masa molowa (M) to ilość masy, jaką zawiera substancja w jednym molu . Jeden mol jest zdefiniowany jako 6,022 * 10 podniesiony do 23 cząsteczek.
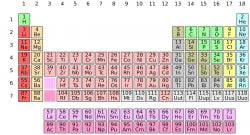
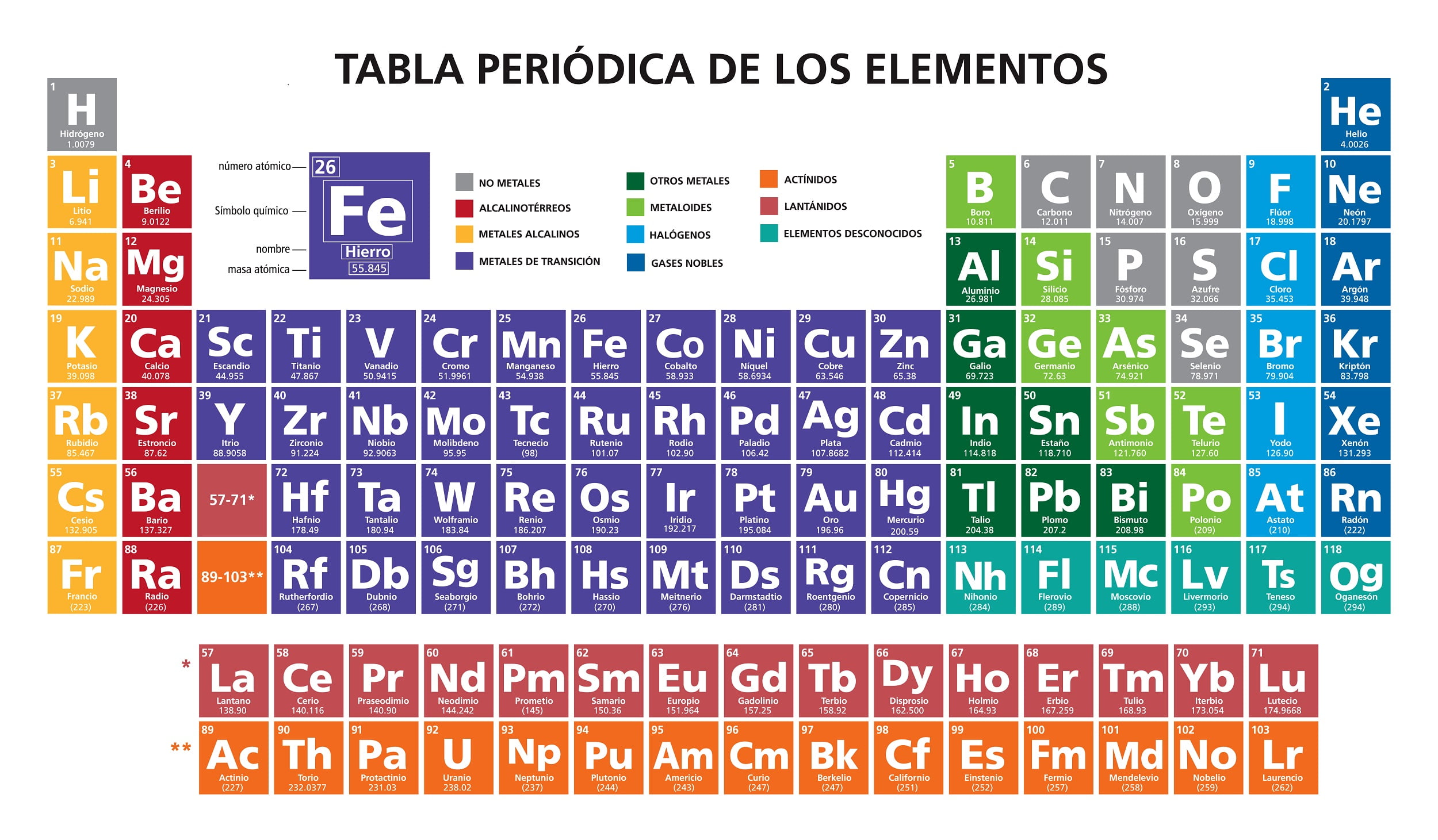
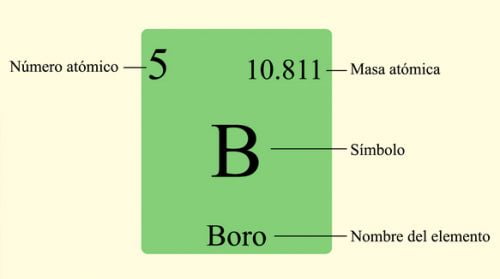
W układzie okresowym, na dole pierwiastka znajdą Państwo masę molową pierwiastków, zwaną również masą atomową lub ciężarem atomowym. Wodór na przykład ma masę cząsteczkową 1,008, a azot ma masę cząsteczkową 14,01.
Patrz również:
- Układ okresowy.
- Pierwiastek chemiczny.
Aby obliczyć masę cząsteczkową związku, zwaną również masą molekularną lub ciężarem cząsteczkowym, takiego jak amoniak (NH3), należy dodać masę molową pierwiastków związku pomnożoną przez liczbę ich występowania, np:
Masa molowa NH3 =
1 molekuła azotu razy jego masa atomowa 14,01 plus 3 molekuły wodoru razy jego masa atomowa 1,008 = (1 * 14,01) + (3 * 1,008) = 14,01 + 3,024 = 43,038 u = 17,03 masa cząsteczkowa = 17,03 gmol masa molowa w amoniaku.
Gdy zna Pan masę molową związku, zna Pan liczbę moli na gram, pamiętając, że każdy mol to 6,022 * 10^23 cząsteczek.
Dlatego znając masę molową można obliczyć liczbę moli w pojemniku za pomocą wzoru: mol= masa molowa masa molowa. Na przykład, w 100 gramach amoniaku (NH3), aby znaleźć ilość moli musimy podzielić 100 17,03 gmol, co daje przybliżony wynik 5,8 mola w 100 gramach amoniaku.
W chemii masa molowa jest ważna dla określenia masy ilości masy, która jest wymagana dla danej substancji, ponieważ nasze wagi są kalibrowane według masy, a nie według masy. Dlatego masę molową wyraża się zazwyczaj w kilogramach na mol (kgmol) lub gramach na mol (gmol).
Patrz również:
- Masa
- Kilogram